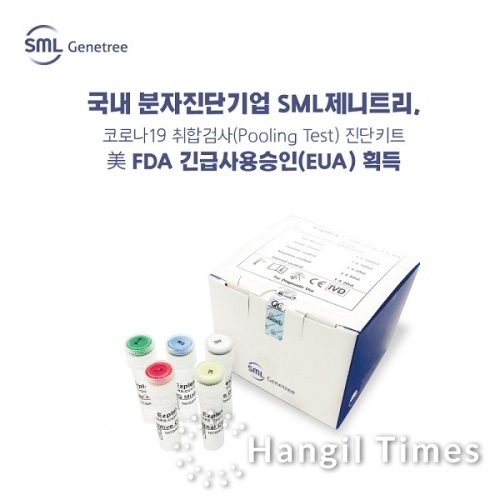
 사진제공=SML제니트리[우성훈 기자] SML제니트리(에스엠엘제니트리)가 국내 바이오 기업 최초로 취합검사(Pooling Test)가 가능한 코로나19 진단키트를 미국 식품의약국(FDA)으로부터 긴급사용승인(EUA) 받았다고 밝혔다.
사진제공=SML제니트리[우성훈 기자] SML제니트리(에스엠엘제니트리)가 국내 바이오 기업 최초로 취합검사(Pooling Test)가 가능한 코로나19 진단키트를 미국 식품의약국(FDA)으로부터 긴급사용승인(EUA) 받았다고 밝혔다.
해당 제품은 기존 국내 업체가 FDA 긴급사용승인을 받은 제품과는 달리 취합검사(Pooling Test)가 가능해 대량의 선별검사에 활용될 수 있다. 취합검사는 5명 단위로 검체를 취합해 검사하고 양성일 경우 개별검사를, 음성일 경우 모두 음성판정을 내는 방식으로 이뤄진다. 특히 다수의 검체를 한 번에 검사하기 때문에 기존 진단키트 대비 높은 민감도와 특이도를 가져야만 해당 검사가 가능하다.
FDA에 의하면 개별검사와 취합검사의 결과비교 테스트에서 100%의 일치도를 보였고 세계에서 20번째, 대한민국 기업으로는 최초로 해당 테스트를 통과한 것으로 알려졌다. 현재 한국을 비롯해 미국, 유럽 등은 취합검사를 통해 대규모 진단검사를 진행 중이다. 이는 감염예방을 위한 주기적인 검사에 효과적이므로 향후 백신과 치료제가 보급된 이후 보편적인 코로나19 검사방법으로 자리잡을 것으로 전망되고 있다.
SML제니트리는 이와 같은 R&D 역량의 경쟁우위와 창사 이후 꾸준히 지속된 높은 매출, 수익 성장성을 바탕으로 내년 상반기 코스닥 상장을 추진할 계획이다. IPO주관사는 미래에셋대우에서 맡아 진행할 예정이다.
SML제니트리 안지훈 대표는 “아직도 심각하게 진행 중인 미국의 코로나19 상황에 취합검사법이 가능한 ‘Ezplex® SARS-CoV-2 G Real-Time PCR Kit’가 좋은 역할을 할 것이라고 기대한다”면서, “SML제니트리는 코로나 진단키트뿐만 아니라 호흡기를 비롯한 다양한 감염증과 암 조기진단 기술 등 분자진단 영역에서 수준 높은 제품 파이프라인을 보유하고 있다. 이번 FDA 긴습사용승인을 기점으로 글로벌 시장에 당사가 보유한 혁신적인 제품을 순차적으로 공급할 계획”이라고 말했다.
[서울시 문화재 119] 서울 홍제동 오층석탑 [박광준 기자] 서울 홍제동 오층석탑은 서울특별시 용산구 국립중앙박물관에 소장된 고려시대 화강암으로 건조한 5층 석조 불탑. 석탑으로, 1963년 보물로 지정됐다. 전체를 화강암으로 건조한 이 석탑은 원래 서울특별시 서대문구 홍제동에 있었으나 시가지 확장으로 1970년 경복궁으로 옮겨왔다. 현재는 용산 새 국립중앙박물관으로 옮겨놓...

 서울시, 정비사업 인허가 기간 확 줄인다...첫 통합심의 통과
서울시, 정비사업 인허가 기간 확 줄인다...첫 통합심의 통과
 [독지기고] 아직도 영농부산물을 태우고 있습니까?
[독지기고] 아직도 영농부산물을 태우고 있습니까?
 클랫폼, 스마트팜 활용 도농 융복합단지 조성 추진
클랫폼, 스마트팜 활용 도농 융복합단지 조성 추진
 KT-경기도 상인협회, 전통시장.소상공인 업무 자동화 협력
KT-경기도 상인협회, 전통시장.소상공인 업무 자동화 협력
 한양대학교병원, ‘2024년 루게릭병 환우를 위한 건강강좌’ 개최
한양대학교병원, ‘2024년 루게릭병 환우를 위한 건강강좌’ 개최
 용인시외국인복지센터, 미얀마 설 맞아 문화 교류의 장 개최
용인시외국인복지센터, 미얀마 설 맞아 문화 교류의 장 개최
 한길타임즈 CG
한길타임즈 CG
 신간 '1880년대 울릉도와 동남제도개척사 관계자료집' 발간
신간 '1880년대 울릉도와 동남제도개척사 관계자료집' 발간
 뉴진스 다니엘, 설레는 눈빛과 비주얼로 ‘마리끌레르 코리아’ 5월호 표지
뉴진스 다니엘, 설레는 눈빛과 비주얼로 ‘마리끌레르 코리아’ 5월호 표지
 대한가라테연맹 ‘2024년 전국 지도자세미나 & 심판 강습회’ 개최
대한가라테연맹 ‘2024년 전국 지도자세미나 & 심판 강습회’ 개최
 北京 덕승문 (德胜门)의 봄!
北京 덕승문 (德胜门)의 봄!

 목록으로
목록으로